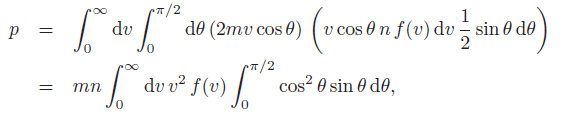我們想知道,在平衡下,有多少分子,其速率是介於 v 與 v + dv 之間,且其方向是在 θ 到 θ+ dθ之間。
認識 固體角
角度如何由孤長與半徑定出?
θ = s / r (見圖)
r 與 s 同步增大,角度不變
立體角
Ω = A / r2
全部範圍是 4πr2 / r2 = 4π
某速度、某方向飛行的分子數
如果分子沿任何特定方向的皆無偏好,則局限在 dΩ 固體角內的分量 (component) 為
dΩ/ 4π
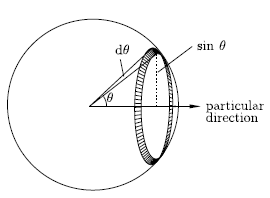
如果已定了某方向,則與該方向呈一夾角,涵蓋 θ到 θ+ dθ範圍的固體角大小(一條環)為
dΩ = 2πsinθdθ
因此,其立體角分量是
dΩ/ 4π = (1/2) sinθdθ
也就是說,(擇定一方向情況下),每單位體積,將有
n f(v) dv (1/2) sinθdθ
這麼多的分子,其速率是介於 v 與 v + dv 之間,且其方向是在 θ 到 θ+ dθ之間。
擊中壁面的分子數
問題解析:
對某一壁面,有其法向量,來自不同之入射角之氣體流,對同一壁面的有效截面並不同,因此氣體數目就會隨角度的不同而不一樣。以下具體推導。
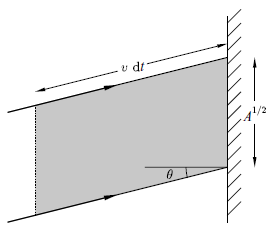
到目前為只,方向是任意指定。現在,把此一方向定為一個面積為 A 之壁面的法方向,見圖 6.5。
在小段時間 dt 之內 ,自角度θ飛來而能覆蓋到壁面 A 之分子流,其掃出來的體積大小為
A v dt cosθ
(亦即角度越大,其有效體積越小)
拿這個體積,去乘上剛才前面得到之符合速率與角度之分子的分量,得
A v dt cosθn f(v) dv (1/2) sinθdθ
也就是說,單位時間內、撞擊到單位面積的,速率在 v 與 v + dv 之間,角度在 θ 到 θ+ dθ之間的分子總數是
v cosθn f(v) dv (1/2) sinθdθ