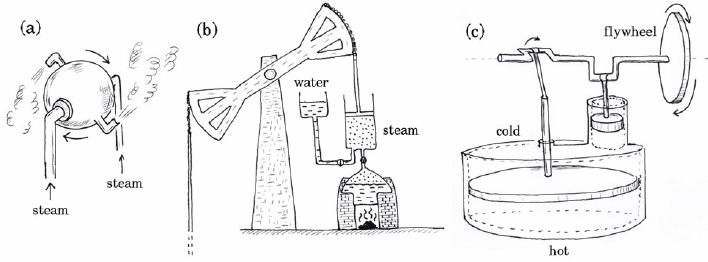
氣體理論(理想氣體方程式)的成功,讓卡諾得以提出簡明的理想引擎,它有兩個最重要的特性:(1) 其由溫差造成熱流中,作功的比例是是可以精確解析計算的,(2) 由於全由可逆過程組成循環,因此也可以反轉。
卡諾引擎之可以反轉的特性,使卡諾可以提出冷、熱機結合的想像實驗。使用"熱不會自動由低溫處流向高溫處" 的常識,推得了 "沒有任何引擎(注意引擎的定義)的效率可以超過卡諾引擎者(事實上是所有可逆者)" 這樣的一個重大的規律。此一觀念催生了熱力學第二定律的建立。
第二定律有好幾種陳述,透過 T 字型熱功三叉路 的有用圖像,可以證明它們都是等效的。
而此一陳述/定律尋求數量化的過程時,便帶出了熵的定義。
本章比較長,其架構如下:
第二定律(含不同陳述)
卡諾引擎及其效率
卡諾定理
克勞休斯、凱爾文陳述的等效性
熱機例
反轉運行的熱機
克勞休斯定理
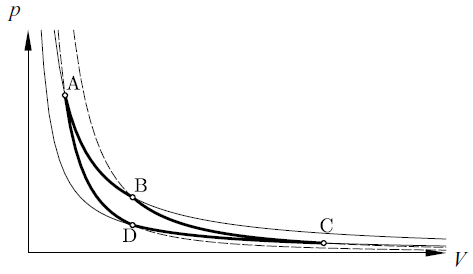
上面 A-B、C-D 是等溫線;A-D、B-C 則是絕熱線。
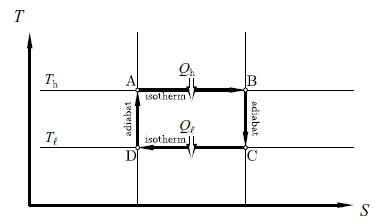
W = Qh - Ql
Ex 13.1 將理想氣體進行卡諾循環的熱流比 Qh / Ql ,以溫度比 Th / Tl 表示出來。
利用前章 12.2 的結果,
A → B : Qh = RTh lm (VB / VA)
B → C : Th/Tl = (VC / VB)γ-1
C → D : Ql = - RTl lm (VD / VC)
D → A : Tl/Th = (VA / VD)γ-1
上四式中的第二、第四式導致
VC / VB = VD / VA
移項得
VB / VA = VC / VD
前四式中的第一式除以第三式,並置換掉體積比值,導致
Qh / Ql = Th / Tl
這樣的一個關鍵的結果。
卡諾引擎之熱流與作功的示意圖
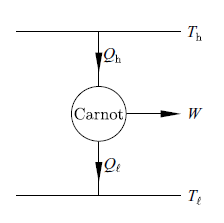
其效率的定義
η ≡ W / Qh
η永遠是一個比 1 小的值,因為所作的功 W 不可能大過 提供的熱量 。
Ex 13.2 卡諾引擎的效率
ηCarnot = (Qh - Ql) / Qh
使用 (13.7) 即理想氣體進行卡諾循環:有 Qh / Ql = Th / Tl,得
ηCarnot = (Th - Tl) / Th = 1 - ( Tl / Th )
真實引擎比起卡諾引擎的效率又低了不少,見下例:
Ex 13.3 渦輪發電機
卡諾(理想極限) 60%、實際 40%。
事實上,卡諾引撉有最高的引擎效率(引擎效率的定義見上),這是一個定理。
卡諾定理
所有連接兩個溫度(熱庫)之間運作的熱機,其 (引擎) 效率不會超過卡諾引擎者。
問題:卡諾引擎的效率之公式形式 1 - Tl / Th 到底有什麼奧妙之處? 何以僅這樣就已經是最高可能的效率?
此定理的證明,可基於克勞修斯陳述,用反證法,巧妙地把一個效率更高的引擎用來反轉卡諾引擎:
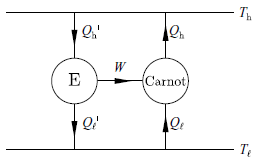
如果存在 E 比 Carnot engine 效率更高,即
ηE > ηCarnot
即
W / Q'h > W / Qh
因而
Qh > Q'h ,也就是說 Qh - Q'h > 0
另外,基於熱力學第一定律,
W = Q'h - Q'l = Qh - Ql
Qh - Q'h = Ql - Q'l
從上面 Qh - Q'h > 0 因此上式等號左邊為正,故等號右邊也是。
但我們仔細看這個 Ql - Q'l 相當於自低溫熱庫 Tl 所抽走的熱量,如果它可以是正的,代表熱力學第二定律己經違反。
(上述的巧妙證明,是卡諾所提出,才催生熱力學第二定律。在未有該定律的當年,卡諾以低溫送熱到高溫有違常識,來確立論點。)
餘定理
所有的可逆引擎皆有相同的效率 ηCarnot
證明:
想像易外一個可逆引擎 R,基於卡諾定理 ηR ≤ηCarnot 。我們將它逆轉並像下圖那樣接上一個卡諾引擎。
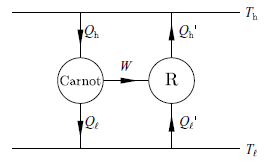
此一架講將會造成熱從低溫傳到高溫的淨效應,因此違反克勞修斯陳述(第二定律),除非其效率不是小於而是相等。如此得證。
對卡諾循環而言,固然熱流 Qh 進 (+)、 Ql 出 (-),熱量並不守恆,但是基於 Qh/Ql = Th/Tl 特性, 有 Qh / Th = Ql / Tl ,也就是說 ΔQ / T 這個量,加總起來(流出帶負號),在一個循環後是守恆的,如下:
Σcycle ΔQrev/T = Qh / Th + (-Ql)/ Tl = 0
換成積分符號的話
∫cycle đQrev/T = 0
(物理學一貫的目標就是在找守恆量,我們在這裏看到一個了嗎?還是只找到了一個狀態函數?)
我們在此之前,僅用卡諾引擎。以下我們想探討一個比較真實的情況,即 (1) 作功之物體一刻系列溫度而非僅兩個。(2) 另外則是,不一定可逆。
假設我們現在有一個循環,在某個過程點 i 上,其熱的進入 đQi (可以是負,後面說明),且當時系統連接到的熱庫是 Ti (如下 (a) 圖),
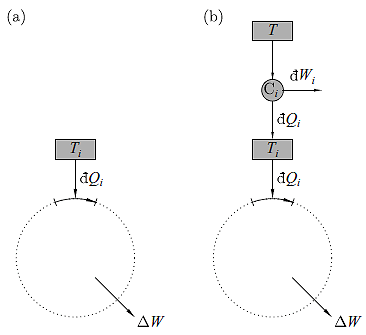
則由於是一個循環的關係,內能繞一圈後不變,而不同階段 i 進進出出的正負總合就等於作功。故基於第一定律本來就有,總功為:
ΔW = Σi đQi
接下來,要把整組機械系統浸在溫度是 T 的環境中,並用最有效率的卡諾引擎收集餘熱作功。想像每個過程點 i 的熱流 đQi 各是由一個連接在溫度 T 及 Ti 熱庫的卡諾引擎所提供(如上圖 (b)), 而這些 T 熱庫則是全部又接在一起 (為什麼要這樣想?)<管控熱庫,儘可能防止熱耗散>,如此,
我們可以寫下各過程點的卡諾引擎作功 đWi ,基於卡諾引擎
"熱流入 Ti 熱庫" / Ti = "熱流出 T 熱庫" / T ,即
đQTi / Ti = đQT / T
再加上,我們有 đQT = đQTi + đWi,故得
đQTi / Ti = (đQTi + đWi)/ T
此 đQTi 事實上在本例中就是 đQi ,故上式變成
đQi / Ti = (đQi + đWi)/ T
即
đWi = đQi (T / Ti - 1)
(在此導出了待會要用的關係式)
我們可看出以上(b) 圖考量的系統,能夠把全部的熱都拿去作功,如此違反了第二定律(違反 Kelvin 陳述),因此上面的結論不可能成立 。
問題:錯誤的前提所推得的結論一定是錯誤的嗎?
(其實,此處課文的邏輯架構是:完全熱轉功之總功已算出,假設大於零,則違反第二定律)
因此上述想像機械總功不是真的可以拿到的,即數學上不可以為正,如此導致 "每個循環的總功" = ΔW + ΣcycleđWi ≤ 0
前有ΔW = Σi đQi,代入,再加以把 đWi 寫成 đQi (T / Ti - 1) ,我們因此有
T Σcycle đQi / Ti ≤ 0
由於 T > 0,我們於是得到
Σcycle đQi / Ti ≤ 0
寫成積分式則成為
∫C đQ / T ≤ 0
Clausius' Theorem 總結如下:
對任何封閉循環,∫C đQ / T ≤ 0 ,其中等號在其為可逆時成立。
(證明就是前面的敘述)
Ex 13.5 兩個具固定熱容值之物體作為熱庫所構成的卡諾循環 (舊版課本沒有)